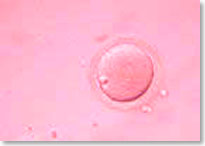
 Después de la supervisión del ciclo y la estimulación de los óvulos mediante medicamentos inyectables, se realiza la recuperación de los óvulos 35 horas después de la inyección de gonadotropina coriónica humana, en un momento en el que los óvulos ya estarán maduros pero aún no se ha producido la ovulación. El método más habitual para realizar esta recuperación en procedimientos de fecundación in vitro es la aspiración guiada por ecografía. La aspiración transvaginal (ATV) se realiza en el Newport Beach Surgery Center.
Después de la supervisión del ciclo y la estimulación de los óvulos mediante medicamentos inyectables, se realiza la recuperación de los óvulos 35 horas después de la inyección de gonadotropina coriónica humana, en un momento en el que los óvulos ya estarán maduros pero aún no se ha producido la ovulación. El método más habitual para realizar esta recuperación en procedimientos de fecundación in vitro es la aspiración guiada por ecografía. La aspiración transvaginal (ATV) se realiza en el Newport Beach Surgery Center.
Durante la aspiración transvaginal, la paciente se colocará en una camilla de examen similar a la que se usa para realizar una citología. El anestesista colocará a la paciente una vía intravenosa (IV) en el brazo. Esta vía se usará para administrar los medicamentos durante el procedimiento. Antes de la aspiración transvaginal, se colocará un espéculo en la vagina para poder limpiarla con soluciones estériles que no dañen los óvulos.
El procedimiento de recuperación emplea una sonda de ultrasonido vaginal con una guía metálica. Esta guía permite colocar una aguja hueca dentro de la sonda. La punta de la aguja tiene unas marcas que la hacen visible en el monitor de ultrasonido. La aguja está fijada a un conducto conectado, a su vez, a un tubo de plástico y a una máquina de succión suave. El médico utiliza la sonda de ultrasonido vaginal para poder ver los ovarios y los folículos que residen en su interior en el monitor. Una vez que la paciente está anestesiada, la aguja se introduce en la pared vaginal, en uno de los folículos del ovario. Cuando la punta de la aguja penetra en la pared del folículo, se activa la máquina de succión. El fluido del folículo se aspira y fluye por el tubo de plástico. El óvulo suele estar ligeramente adherido a la pared interna del folículo y, al extraer el fluido del folículo, el tubo aspira también el óvulo. A continuación, un embriólogo recibe el tubo para examinar cada gota del fluido en un microscopio y detectar un óvulo. Suele ocurrir que algunos folículos no contengan óvulos. Por tanto, el número de folículos puede no ser igual al número de óvulos detectados. El procedimiento concluye cuando se aspiran todos los folículos de ambos ovarios. La pareja deberá proporcionar una muestra fresca de semen el mismo día de la recuperación de óvulos.
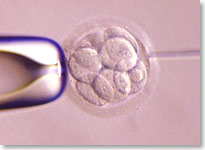
La eclosión asistida es un procedimiento que implica la creación de una pequeña abertura en la capa externa del embrión, la zona pelúcida, cuando dicho embrión ha alcanzado la etapa de entre seis y ocho células. Esta abertura facilita la eclosión de la masa celular después de la transferencia del embrión, un factor que, en teoría, facilita la implantación del embrión y, por tanto, el contacto con el endometrio. Hasta ahora, la eclosión asistida se empleaba en situaciones determinadas: si la paciente tenía más de 40 años, presentaba una zona pelúcida demasiado gruesa o si los demás intentos de fecundación in vitro habían fallado. En la actualidad, la eclosión asistida se realiza en nuestro laboratorio de fecundación in vitro de forma rutinaria para todos los casos de transferencia de embriones. Aunque es cierto que no todas las clínicas de fertilidad que realizan una eclosión asistida obtienen los mismos resultados, es preciso aclarar que existen distintas formas de crear la abertura, desde el uso de una solución acídica hasta la aplicación de un tipo especial de láser. También es importante destacar que el tamaño de la abertura, la forma en la que se transfieren los embriones después de la eclosión y la calidad de dichos embriones en el momento de la eclosión son factores esenciales para lograr el éxito. Hay que aclarar, no obstante, que la eclosión asistida no modifica la composición genética de un embrión individual. Aunque la tasa de implantación general se puede mejorar con la eclosión asistida, la pérdida de un embarazo concreto depende de la edad y viene determinada principalmente por la composición cromosómica de dicho embarazo.
El último paso de un ciclo de fecundación in vitro es la transferencia de embriones al útero. Tradicionalmente, los embriones se transferían entre uno y cinco días después de la recuperación de óvulos. A medida que se han ido conociendo las necesidades fisiológicas del embrión, el día de la transferencia se ha ampliado progresivamente. Algunos embriones con anomalías genéticas dejan de desarrollarse durante los cinco días siguientes a la recuperación de óvulos; por tanto, si se espera más tiempo es posible seleccionar los embriones que presentan más posibilidades de derivar en un embarazo sano. No obstante, no todos los laboratorios de fecundación in vitro disponen de maquinaria para cultivar embriones hasta la etapa de blastocisto (día 5). Lo más importante para ello es el tipo de incubadora utilizada y la experiencia del personal del laboratorio. El día de transferencia de embrión que nosotros preferimos es el día 5. A la hora de seleccionar los embriones que se van a transferir, se tiene en cuenta su aspecto en el microscopio o los resultados de las pruebas genéticas (cribado genético preimplantacional). El número de embriones que se transferirán viene determinado por la edad de la paciente el día de la transferencia. En general, cuanto más mayor sea la mujer y más temprano el día de la transferencia, mayor será el número de embriones transferidos. Una vez seleccionados los embriones, la técnica para transferirlos al útero dependerá de la experiencia del médico.
Durante la evolución de la fecundación in vitro, la transferencia de embriones al útero no ha recibido la misma atención que otros aspectos del procedimiento. Con el paso del tiempo, sin embargo, se ha hecho evidente que quizá sea una de las etapas más importantes y que pueda explicar la diferencia de resultados entre las distintas técnicas que se utilizan. Resulta evidente que es mejor colocar los embriones en el útero de la forma menos traumática posible. También es obvio que los embriones deben transferirse a la zona del útero con más probabilidades de implantación. No obstante, en la mayoría de casos, la transferencia de embriones se realiza mediante un proceso ciego similar a la inseminación intrauterina. Muchos especialistas afirman que el procedimiento de guía del embrión mediante ecografía puede aportar mayores ventajas, dado que la punta del catéter de transferencia es visible y esto garantiza que los embriones se colocan en la ubicación más adecuada. Los resultados estudiados sugieren que una transferencia ciega de embriones puede tener como consecuencia la colocación de los embriones fuera de la cavidad uterina en un 25-30% de los casos.
Por el contrario, las técnicas que emplean guía por ecografía transabdominal con vejiga llena proporcionan tasas de éxito elevadas en la fecundación in vitro. Hemos podido observar que un enfoque transvaginal es más fácil, no requiere vejiga llena y proporciona una localización muy precisa del mejor lugar para colocar los embriones en el útero. El doctor Anderson realizó por primera vez este procedimiento en el año 2000 y pudo probar de forma instantánea la mejora en las probabilidades de embarazo con embriones frescos y congelados. Además, también detectamos un aumento importante en la tasa de implantación de embriones. Este aumento en las tasas de éxito se detectó inmediatamente después de la adopción del método de transferencia guiada por ecografía transvaginal. No había otras variables en ese momento que pudieran explicar este cambio. Médicos de todo el mundo han ido adoptando esta técnica desde que fue descrita originalmente por el doctor Anderson.
Nuestros resultados con este procedimiento se presentaron en la reunión anual de la Sociedad Reproductiva de la Costa del Pacífico (Pacific Coast Reproductive Society) en 2001 por la que se concedió al doctor Anderson el premio Practicing Physician. El artículo que describe esta técnica se publicó en la revista Fertility and Sterility (Fertilidad y esterilidad) de abril de 2002. El doctor Anderson escribió un capítulo en su libro “Embryo Transfer” (Transferencia de embriones) titulado “Transvaginal Guided Embryo Transfer” (Transferencia de embriones transvaginal guiada) que aportaba más datos sobre esta técnica.